本サイトはアフィリエイト広告を利用しています
国民歯みがき粉「2080」の裏切り…“禁止成分”入りなのに製品回収も遅かった
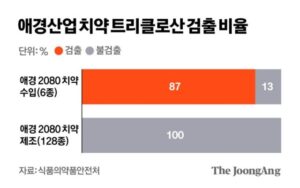
最近、禁止成分の混入問題が浮上した愛敬産業の「2080歯みがき」輸入製品の87%から、禁止成分が検出された。一方、国内製造製品では当該成分は一切検出されなかった。
食品医薬品安全処は20日、ソウル陽川区のソウル地方食品医薬品安全庁で、このような調査結果を発表した。検査対象は、中国のドミ(Domy)社が2023年2月から製造し、愛敬産業が国内に持ち込んだ2080歯みがき6種と、愛敬産業が国内で製造した2080歯みがき128種だ。食品医薬品安全処は関連する論争が提起された後、これら歯みがき134種を回収して検査を行った。
検査の結果、輸入歯みがき6種の870の製造番号のうち、754の製造番号の製品(86.7%)から、禁止成分である「トリクロサン」が最大0.16%まで検出された。食品医薬品安全処によると、問題となった輸入製品の市中流通量は約2900万個で、愛敬産業が当初明らかにした流通量(2500万個)より400万個多い。愛敬産業が国内で製造した2080歯みがき128種からは、トリクロサンは検出されなかった。
輸入歯みがきでトリクロサンが検出された原因は、ドミ社が2023年4月から歯みがき製造設備の消毒・洗浄工程でトリクロサンを使用したことによるものと調査された。食品医薬品安全処バイオ生薬局長のシン・ジュンス氏は「製造設備に残留したトリクロサン成分が歯みがき製品に混ざったことが確認された」とし、「作業者ごとに消毒・洗浄液の使用有無や使用量に差があったため、製品ごとの残留量が一貫しない形で現れた」と説明した。
食品医薬品安全処が愛敬産業に対して現場点検を行った結果、回収に必要な措置が遅れるなど、回収手続きを期限通り守らなかった事実が確認された。「医薬品等の安全に関する規則」によれば、医薬部外品の輸入者は安全性に問題がある事実を知った場合、遅滞なく流通中の製品を回収するか、回収に必要な措置を取らなければならない。さらに、▶海外製造所に対する輸入品質管理の不備 ▶トリクロサンが混入した輸入歯みがきの国内流通 などが確認され、食品医薬品安全処は愛敬産業に対する輸入業務停止などの行政処分手続きを進める方針だ。
トリクロサンは製品の変質を防ぐための保存剤成分で、韓国では2016年から口腔用品への使用が禁止されている。ただし今回トリクロサンが検出された輸入歯みがき製品については、専門家の助言の結果、人体への危害懸念は低い水準と評価された。トリクロサンは体内で速やかに排出され蓄積の懸念が低いこと、欧州など海外では0.3%以下を安全な水準と見なしていることが根拠として示された。
助言に参加した檀国大薬学科のキム・ギュボン教授は、この日のブリーフィングで「欧州や米国など主要国の規制当局は、トリクロサン0.3%以下の製品は危害懸念が低いと判断している」とし、「検出された最大値の0.16%は基準値(0.3%)に達していないため、現在の曝露レベルでは危害評価上の懸念はない」と述べた。
食品医薬品安全処によると、ドミ社は問題発生後、トリクロサンの使用を中止した。また、愛敬産業以外に歯みがき生産を委託した国内外の業者はないことが把握された。
食品医薬品安全処は、輸入歯みがきのトリクロサン検出による国民の不安を考慮し、管理・監督を強化する方針だ。初回の輸入および販売段階では、トリクロサン成績書の提出と、製造番号ごとの自己品質検査をそれぞれ義務化する。
流通段階では、食品医薬品安全処が毎年すべての輸入歯みがきを対象に、トリクロサン含有の有無を全数調査する予定だ。あわせて、有害な医薬部外品の製造・輸入により得た経済的利益を回収するため、懲罰的課徴金を科す法的根拠を整備することにした。食品医약品安全処は「国民が安心できるよう、歯みがきなど医薬部外品の安全管理を強化する」と明らかにした。
引用元記事:https://n.news.naver.com/article/025/0003497812?ntype=RANKING